EL CALOR, EL TRABAJO Y SU RELACION EN LA TERMODINAMICA
Cordiales saludos para toda la comunidad de Hive. Particulares saludos para todos mis Hive-Lectores y Hive-Seguidores. En la presente oportunidad les comparto mi post que he titulado EL CALOR, EL TRABAJO Y SU RELACION EN LA TERMODINAMICA. Tanto el concepto de calor como el de trabajo son de gran importancia en la Termodinámica y, por ende, su completo entendimiento es esencial en el estudio de la misma.
Además de hacer llegar un poco de ciencia a la comunidad de Hive en general, espero con el presente contenido seguir contribuyendo, concretamente, con la formación de aquellos estudiantes que, por el COVID-19, deben seguir sus estudios en casa.
Es pertinente, mis Hive-Lectores, que tengan presentes mis siguientes posts durante el eltudio del actual:

Mis estimados Hive-Lectores, en la vida cotidiana usamos la palabra Calor para referirnos a cuando hay temperatura alta en nuestro derredor. Sin embargo, en la termodinámica este término se define como sigue:

Gif animado realizado por mi persona, @tsoldovieri, usando las aplicaciones Paint y PhotoScape
El Calor 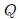 es la transferencia de energía de una parte a otra de un cuerpo (vean la figura 1) o entre diferentes cuerpos (vean la figura 2), en virtud de una diferencia de temperatura (vean al figura 1). es la transferencia de energía de una parte a otra de un cuerpo (vean la figura 1) o entre diferentes cuerpos (vean la figura 2), en virtud de una diferencia de temperatura (vean al figura 1). |
|---|

Gif animado realizado por mi persona, @tsoldovieri, usando las aplicaciones Paint y PhotoScape
Notemos que, en lo anterior, he usado el término Temperatura. Pero ¿qué es la temperatura?
La Temperatura 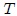 es, macroscópicamente, una magnitud que determina el sentido en que se produce el flujo de calor cuando dos cuerpos se ponen en contacto. es, macroscópicamente, una magnitud que determina el sentido en que se produce el flujo de calor cuando dos cuerpos se ponen en contacto. |
|---|

Gif animado realizado por mi persona, @tsoldovieri, usando las aplicaciones Paint y PhotoScape
El calor es energía en tránsito. Siempre fluye de una zona de mayor temperatura a una zona de menor temperatura, con lo que eleva la temperatura de la segunda y reduce la de la primera, siempre que el volumen de los cuerpos se mantenga constante (vean la figura 3). La energía no fluye desde un objeto de temperatura baja a un objeto de temperatura alta si no se realiza trabajo (del cual hablaré más adelante).
Por tanto, los términos de temperatura y calor, aunque relacionados entre sí, se refieren a conceptos diferentes: la temperatura es una propiedad de un cuerpo y el calor es un flujo de energía entre dos cuerpos a diferentes temperaturas. |
|---|
Por otro lado, mis estimados Hive-Lectores, en Termodinámica:
El Trabajo 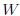 se define como una interacción de energía entre el sistema y su entorno. Es la energía que se transmite de un sistema a otro de tal manera que no esté involucrada directamente una diferencia de temperaturas. se define como una interacción de energía entre el sistema y su entorno. Es la energía que se transmite de un sistema a otro de tal manera que no esté involucrada directamente una diferencia de temperaturas. |
|---|
Este trabajo mecánico, mis amigos Hive-Lectores, es el mismo que se ha estudiado en el curso de Mecánica Newtoniana, es decir, es la transferencia de energía asociada con una fuerza 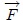 que actúa sobre una partícula a lo largo de un determinado desplazamiento
que actúa sobre una partícula a lo largo de un determinado desplazamiento 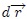 ,
,
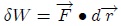
Noten que he escrito 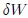 en vez de
en vez de 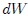 . La diferencia entre los símbolos
. La diferencia entre los símbolos 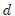 y
y 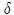 es importante:
es importante:
El símbolo 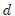 indica una diferencial exacta de una función. Es decir, es una variación que sólo depende del estado inicial y final, no de la trayectoria seguida por la transformación entre ambos. indica una diferencial exacta de una función. Es decir, es una variación que sólo depende del estado inicial y final, no de la trayectoria seguida por la transformación entre ambos. |
|---|
en cambio,
El símbolo 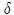 indica una diferencial inexacta de una función. Es decir, es una variación que depende del estado inicial, del final y de la trayectoria recorrida durante la transformación entre ambos. indica una diferencial inexacta de una función. Es decir, es una variación que depende del estado inicial, del final y de la trayectoria recorrida durante la transformación entre ambos. |
|---|
Estimados Hive-Lectores, existen condiciones matemáticas que deben cumplirse para que una diferencial dada sea exacta, las cuales puede consultar el cualquier libro de cálculo integral y diferencial. La integración entre los estados 1 y 2 de una diferencial exacta como 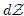 viene dada por,
viene dada por,
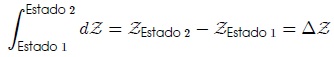
que depende de los mencionados estados y no de la trayectoria seguida por la transformación para pasar entre ellos, es decir, sólo depende de los límites de integración. Por otro lado, la integración entre los estados 1 y 2 de una diferencial inexacta como 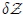 viene dada por,
viene dada por,
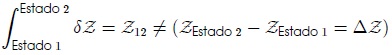
depende de la trayectoria seguida, es decir, no existe una función 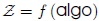 tal que se cumpla una expresión como la (1). De esta manera
tal que se cumpla una expresión como la (1). De esta manera 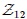 es, simplemente, la suma de los valores de
es, simplemente, la suma de los valores de 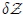 a lo largo de la trayectoria seguida.
a lo largo de la trayectoria seguida.
Gif realizado por mi persona, @tsoldovieri, usando la aplicación Paint
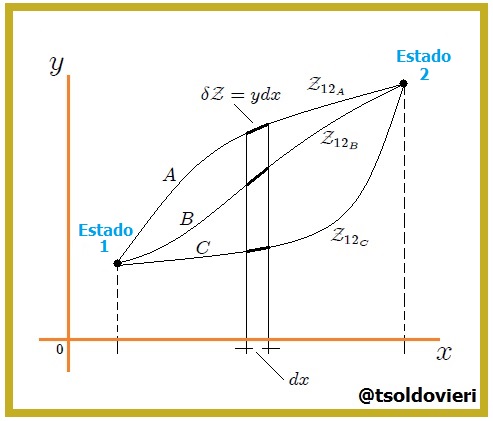
Mis estimados lectores, observen la figura 4. En la gráfica se muestran tres trayectorias 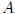 ,
, 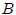 y
y 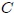 arbitrarias entre los estados 1 y 2, siendo
arbitrarias entre los estados 1 y 2, siendo 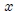 y
y 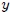 dos variables (
dos variables (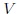 y
y 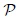 por ejemplo). Con cada pequeño incremento de la trayectoria se asocia una cantidad
por ejemplo). Con cada pequeño incremento de la trayectoria se asocia una cantidad 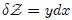 . La suma de estos valores de
. La suma de estos valores de 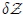 para la transformación global es
para la transformación global es 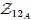 siguiendo la trayectoria
siguiendo la trayectoria 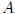 . Una trayectoria distinta entre los estados 1 y 2 como la
. Una trayectoria distinta entre los estados 1 y 2 como la 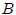 y la
y la 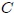 , conduciría a los valores
, conduciría a los valores 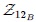 y
y 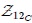 respectivamente, resultando que
respectivamente, resultando que 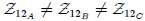 . Notemos, mis amigos Hive-Lectores, que la integración de
. Notemos, mis amigos Hive-Lectores, que la integración de 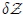 no conduce a la notación
no conduce a la notación 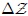 , sino simplemente
, sino simplemente 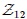 . El valor de una función cuyo diferencial es inexacto, tiene significado únicamente para la transformación global, careciendo de significado para un estado.
. El valor de una función cuyo diferencial es inexacto, tiene significado únicamente para la transformación global, careciendo de significado para un estado.
En general,
(a) El trabajo 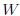 efectuado para llevar un sistema desde un estado 1 a otro 2 depende, no sólo de su estado inicial y final, sino también de la trayectoria seguida por la transformación. (b) La cantidad de calor efectuado para llevar un sistema desde un estado 1 a otro 2 depende, no sólo de su estado inicial y final, sino también de la trayectoria seguida por la transformación. (b) La cantidad de calor 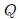 que se suministra o se extrae al llevar un sistema de un estado 1 a otro 2 depende, no sólo de los estados inicial y final sino también de la trayectoria seguida por la transformación. que se suministra o se extrae al llevar un sistema de un estado 1 a otro 2 depende, no sólo de los estados inicial y final sino también de la trayectoria seguida por la transformación. |
|---|
Mis amigos Hive-Lectores, en Termodinámica, cuando una función es función de estado (es decir, es variable de estado
de equilibrio termodinámico), cumple a su vez que:
- Su diferencial total es exacta.
- Su variación en una transformación se puede calcular como el incremento de la función entre los estados inicial y final. Ejemplos: la energía interna
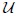 , la energía potencial gravitacional
, la energía potencial gravitacional 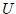 , la presión
, la presión 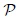 , la temperatura
, la temperatura 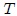 , etc.
, etc.
Por otro lado, cuando una función no es función de estado (no es variable de estado de equilibrio termodinámico, es sólo variable termodinámica), cumple a su vez que:
- Su diferencial total es inexacta.
- Su variación en una transformación no se puede calcular como el incremento de la función entre los estados inicial y final. Ejemplos: el trabajo
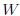 y el calor
y el calor 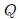 .
.
En general, la diferencial del trabajo es inexacta, siendo exacta sólo cuando 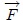 proviene de un campo de fuerzas conservativo. Al integrar (1) resulta,
proviene de un campo de fuerzas conservativo. Al integrar (1) resulta,
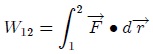
Entre el trabajo 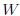 y el calor
y el calor 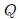 se tiene que:
se tiene que:
- Como la energía es la capacidad para realizar trabajo, entonces existe una relación entre el calor y el trabajo.
- Son manifestaciones externas de energía en tránsito y únicamente se evidencian en las fronteras de los sistemas, apareciendo solamente cuando estos experimentan cambios en sus estados termodinámicos, es decir, cuando ocurren transformaciones termodinámicas.
- Al igual que el calor, el trabajo es una interacción de energía entre el sistema y su entorno. La figura 5 muestra una transformación termodinámica genérica, en la cual se ha definido claramente el sistema y su entorno:

Gif animado realizado por mi persona, @tsoldovieri, usando las aplicaciones Paint y PhotoScape
- Primero el sistema se encuentra en su estado inicial, en equilibrio con su entorno.
- Luego el sistema interactúa con su entorno mediante una transformación termodinámica particular. Durante esta transformación puede entrar o salir energía del sistema en forma de calor y de trabajo. Las flechas que representan el flujo de
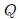 y de
y de  deben cruzar la frontera.
deben cruzar la frontera. - Finalmente, el sistema ha alcanzado su estado final y de nuevo se encuentra en equilibrio con su entorno.
- No son variables o propiedades termodinámicas ya que, a diferencia de las mismas y como se dijo antes, se asocian a una transformación o proceso termodinámico y no con un estado (no tienen significado en un estado). Sus magnitudes dependen de la trayectoria seguida durante una transformación termodinámica así como de los estados inicial y final.
- La descripción completa de su interacción requiere la especificación tanto de su magnitud como de su dirección de flujo. Una forma de hacerlo es estableciendo un criterio de signos. El más empleado es el siguiente: el trabajo que proporciona el sistema es positivo y el que recibe negativo, mientras que el calor suministrado al sistema se considera positivo y negativo el cedido por él. En la figura 6 les ilustro la convención de signos para el calor y el trabajo.

Gif animado realizado por mi persona, @tsoldovieri, usando las aplicaciones Paint y PhotoScape
- Si para el estudio se un sistema en particular la dirección de interacción del trabajo o el calor no es conocida, lo que se hace es suponer una dirección (mediante, por ejemplo, el subíndice entrada o salida) y darle una solución. Un resultado positivo indicará que la dirección supuesta al principio fue la correcta, mientras que un resultado negativo indicará que la dirección es la opuesta.
- A diferencia del trabajo, el calor es una forma de energía que fluye de un cuerpo a otro en virtud de una diferencia de temperaturas. Cuando existe una diferencia de temperatura entre el sistema y su entorno, hay una transferencia de energía como producto de los choques individuales de las moléculas del sistema con las de su entorno. En el caso de que la frontera del sistema sea rígida, la suma de los trabajos debidos a los choques no puede ser expresada como una fuerza por el desplazamiento, sino que es esencialmente lo que se denomina calor.
- Un sistema posee energía pero no trabajo o calor.
- Se reconocen cuando cruzan la frontera del sistema pues ambos son fenómenos de frontera. Si la energía que cruza en un sistema cerrado no es calor, entonces debe ser trabajo.
- El calor es fácil de reconocer, pues la “fuerza” que lo posibilita es una diferencia de temperatura entre el sistema y su entorno. Entonces, es posible afirmar (con cierta simplicidad) que una interacción de energía que no es provocada como la anterior, tiene que ser trabajo.

Gif animado realizado por mi persona, @tsoldovieri, usando las aplicaciones Paint y PhotoScape. Imagen de Calor00102022200002.gif: Alex10pianistderivative work: OSH FPaD (talk) - Calor00102022200002.gif, CC BY-SA 3.0 - Fuente
Los procesos físicos por los que se produce la transferencia de calor son la conducción y la radiación. Un tercer proceso, que también implica el movimiento de materia, se denomina convección. La conducción requiere contacto físico entre los cuerpos (o las partes de un cuerpo) que intercambian calor, pero en la radiación no hace falta que los cuerpos estén en contacto ni que haya materia entre ellos. La convección se produce a través del movimiento de un líquido o un gas en contacto con un cuerpo de temperatura diferente. Vean la figura 7.
Hasta principios del siglo XIX, mis atentos amigos Hive-Lectores, el efecto del calor sobre la temperatura de un cuerpo se explicaba postulando la existencia de una sustancia o forma de materia invisible, denominada Calórico. Según la teoría del calórico, un cuerpo de temperatura alta contiene más calórico que otro de temperatura baja.

Gif animado realizado por mi persona, @tsoldovieri, usando la aplicación PhotoScape. Imágenes de: Thomas Gainsborough - Corel Photo CD, MASTERS I, Public Domain - Fuente & Sir Thomas Lawrence (died 1830), Public Domain - Fuente
El primero cede parte del calórico al segundo al ponerse en contacto ambos cuerpos, con lo que aumenta la temperatura de dicho cuerpo y disminuye la suya propia. Aunque la teoría del calórico explicaba algunos fenómenos de la transferencia de calor, las pruebas experimentales presentadas por el físico británico Benjamin Thompson, Conde de Runford en 1798 y
por el químico británico Humphry Davy en 1799 (vean la figura 8) sugerían que el calor, igual que el trabajo, corresponde a energía en tránsito (intercambio de energía). Entre 1840 y 1849, el físico británico James Prescott Joule (vean la figura 9), en una serie de experimentos muy precisos, demostró de forma concluyente que el calor es una transferencia de energía y que puede causar los mismos cambios en un cuerpo que el trabajo.
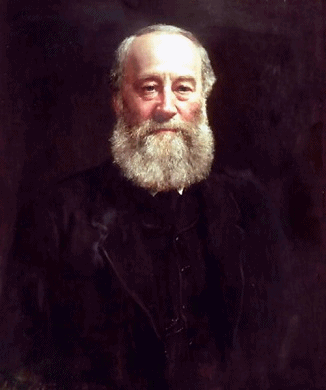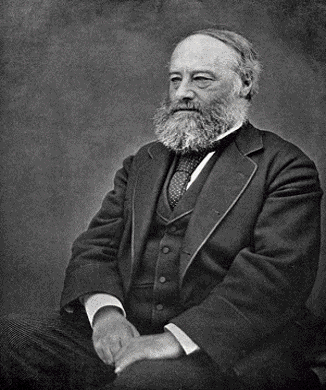
Gif animado realizado por mi persona, @tsoldovieri, usando la aplicación PhotoScape. Imágenes de: John Collier - ssplprints, Public Domain - Fuente & By Henry Roscoe - The Life & Experiences of Sir Henry Enfield Roscoe (Macmillan: London and New York), p. 120, Public Domain - Fuente
Según la Ley de Conservación de la Energía, todo el trabajo mecánico realizado para producir calor por rozamiento aparece en forma de energía en los objetos sobre los que se realiza el trabajo. Esta conexión fue sugerida por Rumford (1798) y calculada por Joule (1845) mediante el siguiente experimento: calentó agua en un recipiente cerrado haciendo girar unas ruedas de paletas y halló que el aumento de temperatura del agua era proporcional al trabajo realizado para mover las ruedas. En la figura 10 les muestro el dispositivo usado en el experimento.
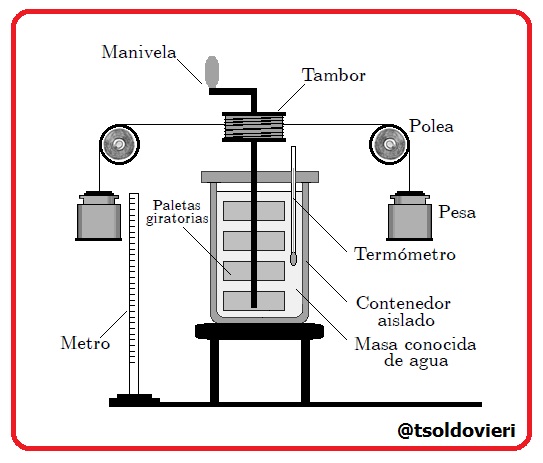
Gif realizado por mi persona, @tsoldovieri, usando la aplicación Paint
La energía mecánica puede convertirse en calor a través del rozamiento y el trabajo mecánico necesario para producir 1 caloría se conoce como Equivalente Mecánico del Calor. A una caloría le corresponden 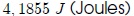 . . |
|---|
En Física, mis amigos Hive-Lectores, la cantidad de calor se expresa en las mismas unidades que la energía y el trabajo, es decir, en Joules, Ergios, etc. Otra unidad cgss es la Caloría (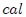 ), definida como la cantidad de calor necesaria para elevar la temperatura de
), definida como la cantidad de calor necesaria para elevar la temperatura de 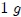 de agua a
de agua a 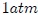 de presión desde
de presión desde 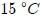 hasta
hasta 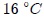 .
.

BIBLIOGRAFIA RECOMENDADA
Aquí les presento 7 textos que recomiendo si desean ahondar en el tema:
Soldovieri C., T. FISICA GENERAL - UNA INTRODUCCION A LOS FLUIDOS, VIBRACIONES Y TERMODINAMICA. Preprint, 2020. El borrador se puede descargar desde mi web www.tsoldovieritsweb.ihostfull.com
Bauer, W. & Westfall, G. D. FISICA PARA INGENIERIA Y CIENCIAS, volume 1. McGraw-Hill/Interamericana de México, S. A. de C. V., 2011.
Bueche, F. J. & Hecht, E. FISICA GENERAL. Schaum. McGraW-Hill / Interamericana Editores, S.A. de C.V., México, 10ma edition, 2007.
Fishbane, P. M.; Gasiorowicz, S. G. & Thornton, S. T. PHYSICS FOR SCIENTISTS AND ENGINEERS WITH MODERN PHYSICS. Pearson Education Inc., 3th edition, 2005.
Burbano de E., S.; Burbano G., E. & Gracia M., C. FISICA GENERAL. Editorial Tébar, S.L., 2003.
Halliday, D.; Resnick, R. & Krane, K. S. FISICA, volume 2. Compañía Editorial Continental, S.A. de C.V., México, 4ta edition, 1994.
Hewitt, P. G. CONCEPTOS DE FISICA. Editorial Limusa, México, 1era edition, 1992.


Estimados amigos Hive-Lectores. Espero que la anterior información les sea de mucha utilidad. Si tienen preguntas, no duden en hacérmelas llegar pues, con mucho gusto, les atenderé. Igualmente, si tienen detalles que puedan nutrir o mejorar la anterior información, por favor, háganmelas saber. Hasta la siguiente parte del presente post ¡Saludos a todos! 😁.
LES INVITO VISITAR MI WEB PERSONAL www.tsoldovieritsweb.ihostfull.com
En esta página web podrás conseguir los borradores de los libros de texto que estoy escribiendo y varias listas de problemas con respuestas de: Optica, Mecánica Clásica, Mecánica Cuántica, Física General 1, Física General 2 y Física General 3. También encontrarás enlaces a otras páginas web de interés.
Deja tus comentarios en el libro de visitas! 😁

Greetings!
👊😎
@tipu curate
Upvoted 👌 (Mana: 6/18)
Muchísimas gracias @tipu por el apoyo que brindaste a mi post. Muy agradecido. Mis más cordiales saludos.
Mil gracias @dirapa por el apoyo que me brindaste en el presente post. Muy agradecido de verdad. Mis atentos saludos.
Que buen trabajo amigo @tsoldovieri, un contenido muy completo, que sin duda alguna será de gran ayuda, para los estudiantes en el período de cuarentena. Saludos !
Gracias amigo @amestyj. Me alegra que te haya gustado mi post. Es un granito de arena para contribuir. Mis saludos cordiales.
Bastante completa esta 3ra parte profesor @tdoldovieri. Estan geniales los gifs complementan muy bien la información teórica y ayuda a comprender fácilmente todo el contenido. Gracias `por esto!
Muchas gracias @carloserp-2000. Me siento halagado por el piropo en referencia a mis gifs, los cuales aprendí (y continuo aprendiendo) a hacer gracias a las exigencias de calidad en esta comunidad. Aclaro que el presente post es un tema aparte de mis 3 posts anteriores (tres partes de un mismo tema). Mis cordiales saludos hermano.
Amigo @rbalzan79 muchas gracias por tomarte un tiempo para visitar mi post y gracias por la alentadora referencia a mis gifs, los cuales continuo mejorando con la experiencia que me aporta el continuo trabajo en ellos. Mi saludos cordiales.
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider supporting our funding proposal, approving our witness (@stem.witness) or delegating to the @stemsocial account (for some ROI).
Please consider using the STEMsocial app app and including @stemsocial as a beneficiary to get a stronger support.
Thanks for the support @steemstem
Gracias por considerar mi trabajo @mayvileros. Muuuy agradecido por su apoyo, Cordiales saludos.
A su orden, muy buen trabajo el que realiza. Saludos.✌❣🤗
Excelente material profesor @tsoldovieri, aun cuando no es mi área de formación, la incorporación de los Gif animados, hace que la entrega sea muy didáctica. Felicitaciones.
Muchas gracias amigo @lupafilotaxia por pasar, comentar y apoyar mi post. Tu comentario me anima a seguir mejorando mis gifs. Un cordial saludo.
Muy completa su publicación, las ilustraciones son excelentes para complementar el texto. Felicidades por este material de calidad en el campo de la termodinámica, seguramente será muy útil para todo estudiante que investigue sobre este tópico en la web. Saludos @tsoldovieri
Gracias amigo @acont por pasar por mi post. Gracias por tu halagador comentario. Un cordial saludo.