Procesos químicos para obtener semiconductores usados en celdas solares
Saludos mis estimados amigos de la comunidad científica #stem-espanol
Para mejor visualización: blog de iamphysical
Sigo trabajando en mis proyectos de investigación, con la finalidad de fabricar un prototipo de celda solar que tenga una eficiencia de conversión de energía solar fotovoltaica a energía eléctrica con valores mayores al 3%, es mi meta como punto de partida. En el INZIT y el IVIC ya se tenía el trabajo bastante adelantado y los métodos de deposición de películas delgadas estaban bajo protocolo de ejecución satisfactorio. Sin embargo, al llegar a los laboratorios de distintas universidades en Chile, la infraestructura tecnológica estaba direccionada hacia otras líneas de investigación y he tratado de hacer las adaptaciones correspondientes para llevar a feliz término los planes de fabricar un dispositivo optoelectrónico.
Por ejemplo, la síntesis del material absorbente debe transformarse desde los lingotes de semiconductores masivos hacia las nanopartículas que involucre procesos rápidos y económicos para poder escalar en la fabricación de dispositivos fotovoltaicos. Por este motivo, continúo realizando ensayos de síntesis del p-CuInSe2 para optimizar los procesos de obtención del material absorbente, así como de las otras capas constituyentes de una celda solar: material ventana (n-ZnO) y la capa amorticuadora (n-CdS).

Cristales de CuInSe2 obtenidos por síntesis solvotermal.
El procedimiento es relativamente fácil de seguir, se basa en procesos químicos con reactivos de alta pureza colocados dentro de un contenedor de teflón que se encapsula al interior de un reactor o bomba de digestión ácida, conocida en los laboratorios de Venezuela como Bomba Parr.

Procedimiento
Método Solvotermal: Se realizó el primer ensayo de síntesis del CuInSe2 usando el método Solvotermal con los siguientes materiales y equipos:
- Selenio elemental (Se, Aldrich, lot MKCH4169) 99,99 %
- Cloruro de Cobre (I) (ClCu, BiosLab Chile, lote WE8829) 90,0%
- Cloruro de Cobre (II) dihidratado (Cl2Cu·2H2O, Sigma, lot BCBZ9334) 99,0%
- Cloruro de Indio (III) tetrahidratado (Cl3In·4H2O, Aldrich, lot MKCG6933) 97,0%
- Etilendiamina (C2H8N2, Sigma, lot STBG6037V) ⥸ 99%
- Recipiente de digestión ácida Parr Volumen: 450 ml y 200 ml
- Masa de Se: 0,00128 mol * 78,96 g/mol mSe = 0,1011 g
- Masa de Cl2Cu·2H2O: 0,00064 mol * 170,48 g/mol mCl2Cu = 0,1091 g
- Masa de ClCu: 0,00064 mol * 99,00 g/mol mClCu = 0,0634 g
- Masa de Cl3In·4H2O: 0,00064 mol * 293,24 g/mol mCl3In = 0,1877 g
- Volumen de C2H8N2: 9,15 ml
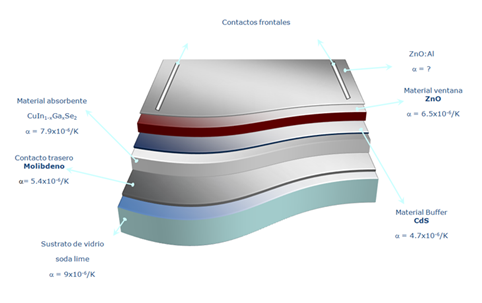
¿Recordamos la configuración de la celda solar?

Por ahora, estoy satisfecho con presentar estas fotografías y videos que servirán como soporte audiovisual para futuros ensayos de síntesis. En otras publicaciones presentaré algunos tips sobre el proceso de síntesis y mostraré algunos resultados experimentales.

El más conveniente: Cu+1 o Cu+2
Los estados de valencia del elemento Cobre (Cu) nos proporcionan información sobre el nivel Cu 2p y de esta manera determinar la energía de enlace del Cu+1 o Cu+2 para la formación del semiconductor CuInSe2. El análisis de un espectro mediante la técnica X-ray photoelectron spectroscopy (XPS) sería útil para llegar a una conclusión efectiva sobre el uso del ClCu o Cl2Cu en la síntesis del material absorbente.

Aportes de esta publicación.
La preparación de los materiales semiconductores que forman parte estructural de cualquier dispositivo optoelectrónico debe cumplir con los mínimos criterios de reproducibilidad y eficiencia para el uso masivo en la industria de la tecnología, por lo cual se requiere la optimización de los procesos de síntesis que garanticen la estabilidad de las propiedades físicas y químicas del material obtenido. Esta es una de las etapas que pretendo alcanzar cuando utilizo diferentes reactivos (ClCu y Cl2Cu) en los ensayos preliminares de síntesis del material absorbente CuInSe2. Hasta una próxima entrega de información y conocimiento científico para mis estimados compañeros de #stem-espanol.

Bibliografía y lecturas recomendadas:
○ Un método sencillo para la obtención de nanoóxidos○ Synthesis and characterization of CuInS2 produced by the method solvothermal
○ Síntesis Solvotermal
○ X‑ray Photoelectron Spectroscopy of Isolated Nanoparticles
En nuestra comunidad se promocionan y valoran las publicaciones de alto impacto relacionados con Ciencia, Tecnología, Ingeniería y Matemáticas, dale clic a la etiqueta #stemsocial, para que te enteres de nuestro trabajo de calidad científica!


Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider delegating to the @stemsocial account (85% of the curation rewards are returned).
Thanks for using the STEMsocial app, which gives you stronger support. Including @stemsocial as a beneficiary could yield even more support next time.