Reacción química. Reactivo limitante y reactivo en exceso
¡Hola estimados amigos y comunidad científica de Hive!
En estos días que pasamos más tiempo en nuestra casa, y tal vez en la cocina porque nos provoca comer algo casi a cada rato, podemos ver la ejemplificación de ciertos conceptos químicos que están presentes en la mayoría de las situaciones que se nos presentan a diario.
Por ejemplo, analicemos lo siguiente:
La preparación de un sándwich relleno con jamón el cual podemos representar por la siguiente ecuación:
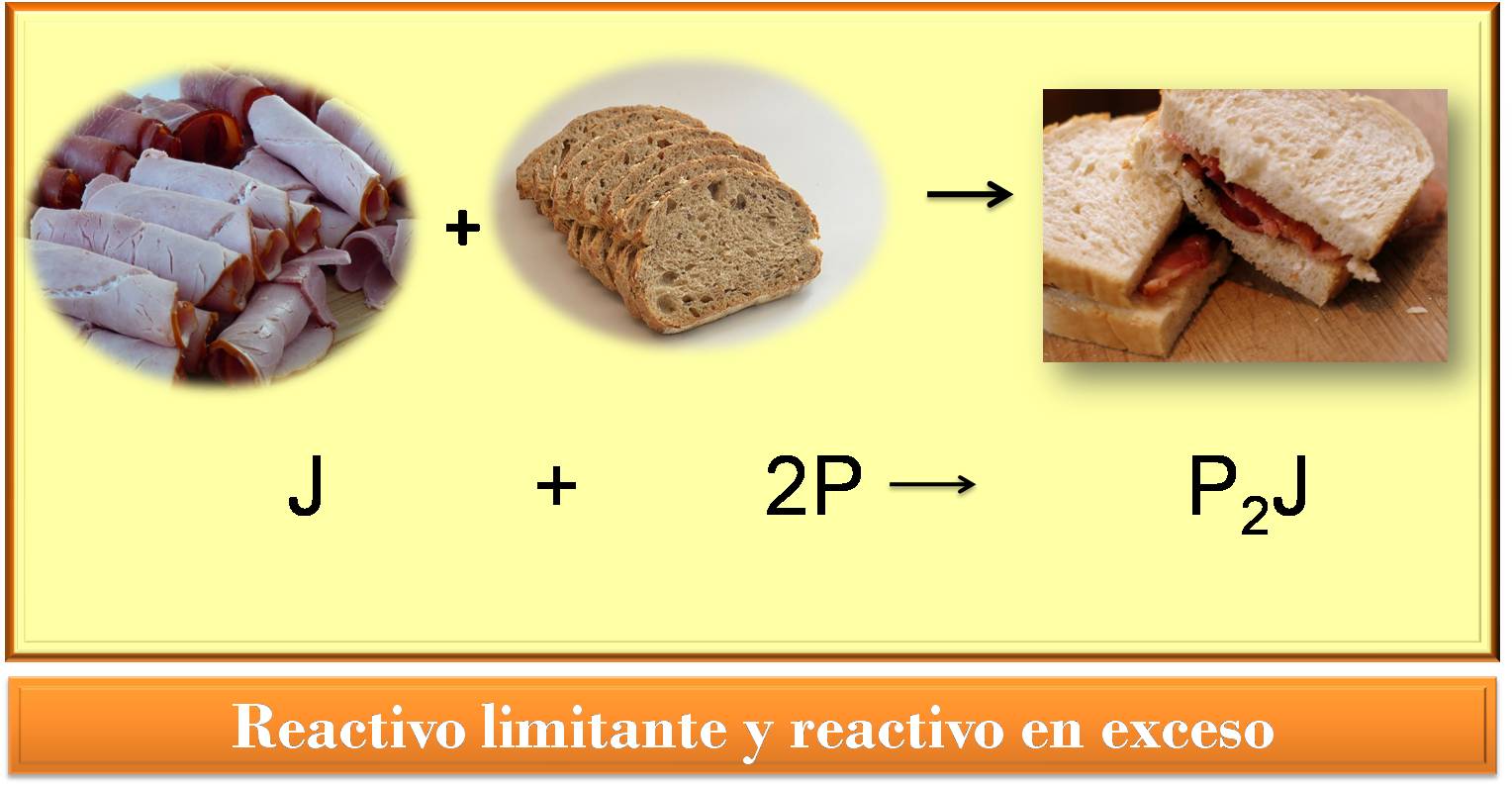
Imagen diseñada por @yusvelasquez, contiene imágenes de dominio público:1, 2, 3
Ahora bien, en función a ello podemos responder las siguientes preguntas:
Si solo se tienen 20 rebanadas de jamón y 8 rebanadas de pan. ¿Cuántos sándwiches se pueden rellenar? ¿Sobra algo? ¿Cuánto?
Podemos observar que solo será posible preparar 4 sándwiches, por lo que nos sobrarán 16 rebanadas de jamón.
Entonces, ¿qué relación hay entre la preparación de los sándwiches y una reacción química?
Este es uno de los ejemplos típicos que nos permite tener una idea acerca de las definiciones de reactivo limitante y reactivo en exceso en una reacción química. En este caso el reactivo que nos limita la reacción es el pan y el que tenemos en exceso es el jamón.
Cabe resaltar que muchas veces el estudio de la estequiometría implica la comprensión de fundamentos teóricos como la formulación química, reacción química, ecuación química, reactivos y productos, balanceo de ecuaciones químicas, que resultan difíciles de manejar, por ello se suelen emplear las analogías como una estrategia de enseñanza.
Por lo que de allí se derivan las siguientes definiciones:
El reactivo limitante es el que se consume por completo en una reacción química. Mientras que el otro es el reactivo en exceso.
¿Como identificar el reactivo limitante en una reacción química?
Esto se puede lograr empleando dos métodos, los cuales los describiremos a continuación.

Principio del método: se basa en el uso de la relación estequiométrica de la reacción química para determinar si hay suficiente de un reactivo para reaccionar con el otro.
Cálculos a realizar: Para realizar los cálculos correspondientes vamos a emplear como ejemplo, la reacción entre el metano y el oxígeno para la formación de dióxido de carbono y agua
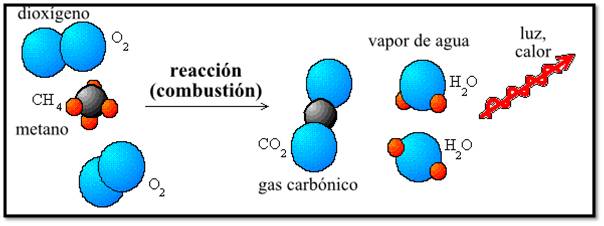
Fuente: wikimedia commons
Supongamos que se tienen las siguientes cantidades: 8 gramos de metano y 48 gramos de oxígeno. La pregunta que debemos responder es ¿quién limitará la reacción? ¿Cuánto de producto máximo se puede obtener con estas cantidades de reactivos?
Para responder esta pregunta, lo primero que se debe hacer es interpretar la información que nos proporciona la reacción
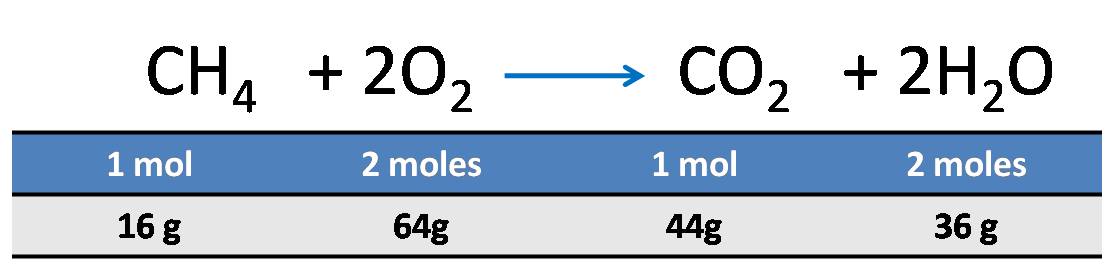
Esta reacción nos dice que para que se lleve a cabo es necesario que reaccione 1 mol de metano con 2 moles de oxígeno. Esto equivale también a que 16 gramos de metano necesitan reaccionar con 64 gramos de oxígeno.
Ahora, basados en las cantidades que nos proporcionaron anteriormente calculemos la cantidad de reactivos que tenemos expresados en moles
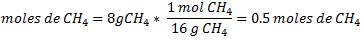
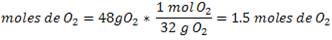
La reacción indica que la relación que debe existir entre los reactivos es
Pero realmente tenemos
De ello se deduce que se necesita el doble de moles de oxígeno por cada mol de metano que se tenga. En este caso para que reaccionen 0.5 moles de metano se necesita 1 mol de oxígeno, así que una vez que reaccionen 0.5 moles de CH4 la reacción se detendrá porque se agotará el CH4 y quedarían aún 0.5 moles de O2 en exceso.
Por tanto,
El reactivo limitante es el CH4
El reactivo en exceso es el O2
¿Cuánto de producto se puede obtener?
Este cálculo se realiza en función al reactivo limitante
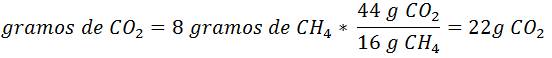

Principio del método: se basa en calcular el peso necesario de uno de los reactivo para que reacciones con una cantidad dada del otro.
Cálculos a realizar: Emplearemos la reacción anterior, y calcularemos la cantidad de oxígeno que reaccionará con 8 gramos de metano, se tiene entonces
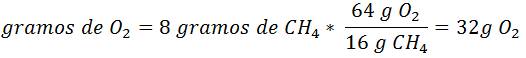
Este resultado nos indica que 8 gramos de metano reaccionan con 32 gramos de oxígeno y se tienen 48g de oxígeno, por lo que se deduce que
El reactivo limitante es el CH4
El reactivo en exceso es el O2
Como vemos, empleando cualquiera de los métodos es posible determinar cuál de los dos reactivos esta en exceso y cual nos limitará la reacción.
La importancia de determinar el reactivo limitante en una reacción radica en que este nos proporcionará información relacionada con el rendimiento máximo de una reacción, o sea lo que se puede obtener de producto. En la realidad, la mayoría de las veces cuando llevamos a cabo una reacción química los reactivos no se combinan en cantidades exactas e iguales, es decir, en las proporciones que se tienen en la ecuación química balanceada, eso trae como consecuencia que al final se puede recuperar uno de los reactivos y otros se pueden consumir por completo. El conocimiento de las reacciones químicas y su estequiometria, es parte fundamental de los procesos industriales. Para llevar a cabo la elaboración de un producto es necesario el cálculo de las cantidades de materia prima que se debe utilizar y estimar la cantidad de producto a obtener, así como también los costos asociados al proceso.
¡Hasta aquí por los momentos, espero sea muy útil la información que les presento!
Referencias bibliográficas
- Whitten K. y Gailey, K. (1985). Química General. México: Nueva Editoral Interamericana
- Atkins, P. y Jones, L. (2006). Principios de Química. Los caminos del descubrimiento. Buenos Aires: Médica Panamericana
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider supporting our funding proposal, approving our witness (@stem.witness) or delegating to the @stemsocial account (for some ROI).
Please consider using the STEMsocial app app and including @stemsocial as a beneficiary to get a stronger support.
Congratulations @yusvelasquez! You have completed the following achievement on the Hive blockchain and have been rewarded with new badge(s) :
Your next target is to reach 600 replies.
You can view your badges on your board and compare yourself to others in the Ranking
If you no longer want to receive notifications, reply to this comment with the word
STOPCheck out the last post from @hivebuzz: