Propiedades, obtención y usos del Bicarbonato de sodio
¡Hola estimados amigos de la comunidad científica de Hive!
Como sabemos en la elaboración de muchos postres y en el campo de la repostería se utiliza un ingrediente muy conocido, cuyo nombre es Bicarbonato de sodio, este compuesto químico posee una gran variedad de aplicaciones por lo que es muy versátil, es por ello que en este post les quiero mostrar información relacionada con sus propiedades físicas y químicas, obtención y otros usos que permitirá conocerlo aún más. ¡Les invito a leer!

@yusvelasquez
La fórmula molecular del bicarbonato de sodio viene dada por NaHCO3, también es conocido como carbonato ácido de sodio o bicarbonato sódico y posee una masa molar de 84 g/mol.
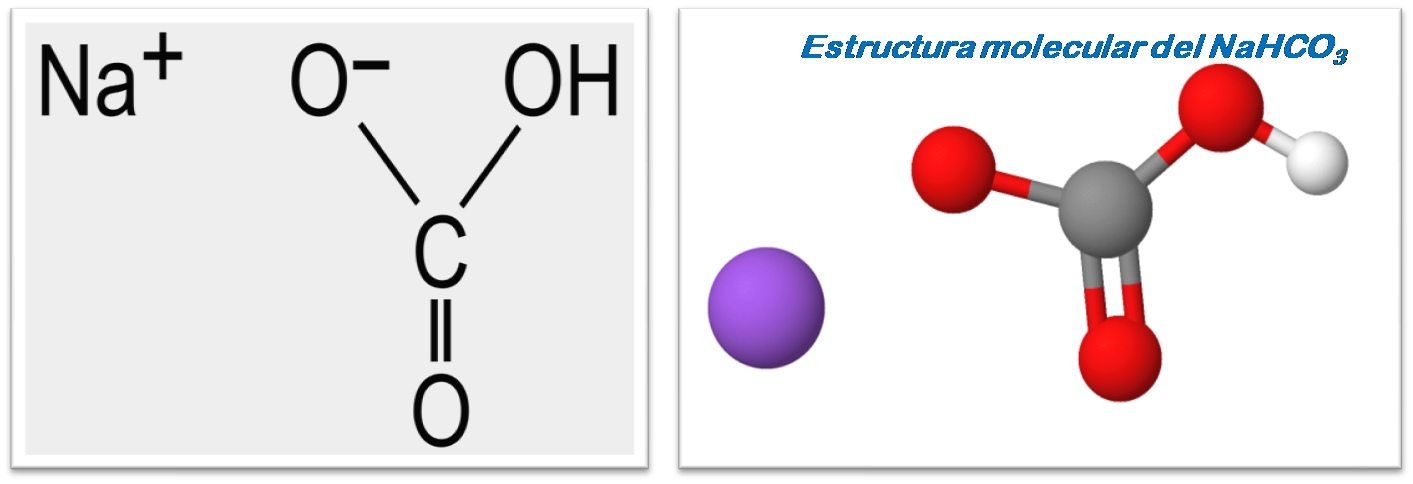
Molécula del bicarbonato de sodio. Fuente:1,2
El bicarbonato de sodio físicamente se caracteriza por ser un sólido de color blanco, con una solubilidad en agua de aproximadamente10,3 g/100g de H2O y posee un ligero sabor alcalino.

Aspecto físico del bicarbonato de sodio. Fuente: @yusvelasquez
Entre sus características destaca la reacción con ácidos en donde se produce CO2 y agua lo que permite ser empleados para muchos fines industriales.
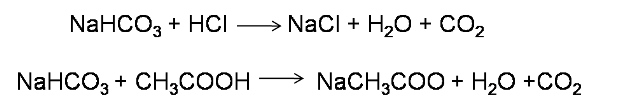

Reacción del bicarbonato de sodio con ácido acético. Fuente:@yusvelasquez
Naturalmente el NaHCO3 se puede encontrar como mineral conocido como nahcolita, perteneciente a la clase de los minerales carbonatos y nitratos.

Mineral Nahcolita: Fuente:wikimedia.org
A nivel industrial se puede obtener por medio de un proceso conocido como Solvay, patentado en 1861 y empleado en la actualidad, donde se obtiene como un producto intermedio en la síntesis del carbonato de sodio Na2CO3, basado en una reacción entre el cloruro de sodio y el carbonato de calcio siendo estas materias primas abundantes y de bajo costo por lo que se emplean para la obtención de carbonato de sodio y cloruro de calcio. La reacción general viene dada por:

Debido a la baja solubilidad del carbonato de calcio, este proceso no se puede llevar a cabo directamente por lo que consta de varias etapas, lo que permite la obtención del bicarbonato de sodio.
Básicamente el proceso solvay, implica reacciones ácido/base y reacciones de precipitación lo que presenta la ventaja que los productos que se obtienen en la etapa intermedia se pueden reciclar o emplear en las etapas siguientes. Este proceso es considerado un ciclo cerrado ya los compuestos de entrada y salida son los indicados en las reacciones, se conoce también como un tratamiento de una disolución acuosa de salmuera amoniacal con dióxido de carbono.
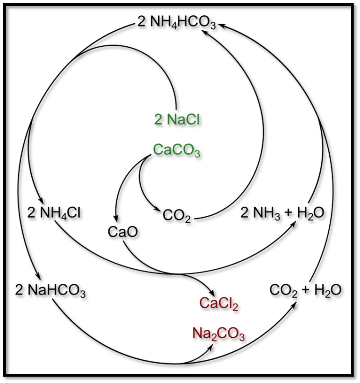
Proceso Solvay. Fuente:wikipedia.org
A continuacion se describirá las etapas del proceso, especificamente se detallará donde se forma el bicarbonato de sodio. Las etapas del método consisten en:
Obtención del bicarbonato de sodio
En esta etapa el dióxido de carbono se hace pasar a través de una solución saturada de NaCl con NH3 en disolución acuosa, precipitando el bicarbonato de sodio que luego se separa de la solución de NH4Cl por filtración. La reacción general es
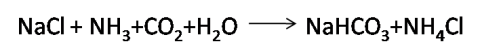
Un esquema de la obtención del bicarbonato de sodio es el que se muestra a continuación
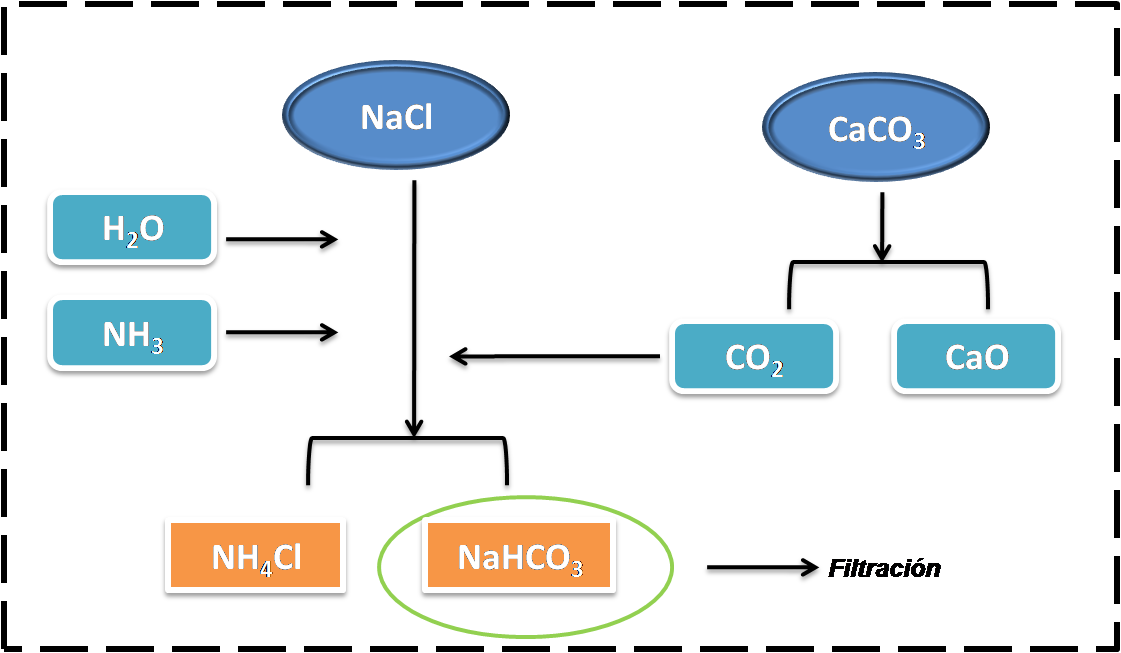
Etapa del proceso solvay donde se forma el bicarbonato de sodio. Fuente:@yusvelasquez
Como se observa en la figura, la calcinación del carbonato de calcio origina el dióxido de carbono para la carbonatación de la salmuera según la siguiente reacción
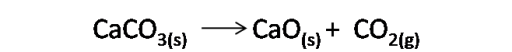
A su vez en esta etapa en primer lugar, el dióxido de carbono reacciona con el amoníaco disuelto y se forma bicarbonato amónico.
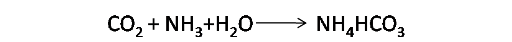
Seguidamente el bicarbonato amónico reacciona con la solución saturada de sal precipitando el bicarbonato sódico y queda en solución el cloruro de amonio.

El proceso Solvay se completa cuando el bicarbonato de sodio obtenido se calcina para obtener el carbonato de sodio. Cabe destacar que actualmente aún se está en la búsqueda de nuevos procedimientos que disminuya el costo del amoníaco, por ser el reactivo más costoso que se emplea en el proceso.
Aplicaciones
A nivel industrial el bicarbonato de sodio es muy empleado, en la industria alimentaria, se emplea en repostería ya que permite el aumento de tamaño de las mezclas otorgándoles el sabor y volumen característicos de cada producto preparado ya que su reacción con otros componentes permite la liberación de CO2. En la industria de la cosmética se usa en variedad de productos para el cuidado de la piel, en desodorantes, lociones, entre otros.
En los productos de limpieza el hogar posee un gran poder, y es utilizado en la formulación de detergentes, desengrasantes, mejora la eficiencia del jabón. En la industria farmacéutica está presente en los antiácidos, productos de cuidado dental.
Adicionalmente está presente entre los compuestos químicos de los extintores ya que ayuda a reducir la cantidad de oxígeno que alimenta al fuego evitando su propagación.
En el hogar es muy empleado en las actividades de limpieza para eliminar los platos, ollas, sartenes, dar brillo a los utensilios de plata, limpiar los zapatos, pisos, muebles entre muchos otros.

Usos del bicarbonato. Fuente:Imagen realizada en power point con imágenes de domnio público1,2,3,4
Como vemos el bicarbonato de sodio es un compuesto con múltiples usos y que comúnmente está presente en los hogares, es de fácil adquisición y almacenamiento, sin embargo, antes de consumirlo o utilizarlo es necesario buscar información necesaria.
¡Hasta aquí el presente post, espero les sea muy útil, gracias por leer!
Referencias
- Bicarbonato de sodio
- Bicarbonato de sodio. wikipedia.org
- Rodríguez, J. y Rodríguez D. Los procedimientos clásicos de la fabricación de la sosa
- 50 Asombrosos Usos y Beneficios del Bicarbonato de Sodio. Boguía
The sodium bicarbonate is very important even for cooking! Thanks for the explanation
!1UP
<a href="https://discord.gg/zQrvxAu7mu"> <img src="https://files.peakd.com/file/peakd-hive/thecuriousfool/23wCNFDyCLJu1v77TTg2MYKkd7XWkgF9fhiLujTDAaLaUz7H4AaQkDentB5UMVS8FcrVs.png"></a>You have received a 1UP from @gwajnberg!
@stem-curator
And they will bring !PIZZA 🍕.
Learn more about our delegation service to earn daily rewards. Join the Cartel on Discord.
PIZZA Holders sent $PIZZA tips in this post's comments:
@curation-cartel(8/20) tipped @yusvelasquez (x1)
Learn more at https://hive.pizza.
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider delegating to the @stemsocial account (85% of the curation rewards are returned).
You may also include @stemsocial as a beneficiary of the rewards of this post to get a stronger support.
Siempre recuerdo que en la escuela se hacían experimentos con este compuesto, así como explicas, un volcán / simular la acción de la lava, al mezclar vinagre + bicarbonato
Congratulations @yusvelasquez! You have completed the following achievement on the Hive blockchain and have been rewarded with new badge(s):
Your next target is to reach 70000 upvotes.
You can view your badges on your board and compare yourself to others in the Ranking
If you no longer want to receive notifications, reply to this comment with the word
STOPCheck out the last post from @hivebuzz:
Support the HiveBuzz project. Vote for our proposal!
¡Felicitaciones!
Estás participando para optar a la mención especial que se efectuará el domingo 11 de septiembre del 2022 a las 8:00 pm (hora de Venezuela), gracias a la cual el autor del artículo seleccionado recibirá la cantidad de 1 HIVE transferida a su cuenta.
¡También has recibido 1 ENTROKEN! El token del PROYECTO ENTROPÍA impulsado por la plataforma Steem-Engine.
1. Invierte en el PROYECTO ENTROPÍA y recibe ganancias semanalmente. Entra aquí para más información.
2. Contáctanos en Discord: https://discord.gg/hkCjFeb
3. Suscríbete a nuestra COMUNIDAD y apoya al trail de @Entropia y así podrás ganar recompensas de curación de forma automática. Entra aquí para más información sobre nuestro trail.
4. Visita nuestro canal de Youtube.
Atentamente
El equipo de curación del PROYECTO ENTROPÍA
Congratulations your publication has been chosen among the best of the day.
KEEP CREATING GOOD CONTENT.