Estudio de casos de soluciones salinas y cálculo de pH
¡Hola estimados amigos!
Vamos a partir de la reacción de neutralización, en la cual participa un ácido y una base y cuyo producto está formado por una sal y agua.

Si le medimos el pH a la solución salina formada puede que éste sea neutro, ácido o básico. Aquí es donde debemos recordar que según la teoría de Bronsted y Lowry, un ion puede actuar como un ácido o como una base, y por tanto el pH de la solución salina va a depender de la acidez o basicidad de sus iones correspondientes y la tendencia que éstos tengan a hidrolizarse, entendiéndose como reacción de hidrólisis aquella que se lleva a cabo con el agua.
En función a ello, existen cuatro tipo de sales, comenzaremos con el estudio de dos casos en este post, dejando los otros dos para abordarlos en una segunda parte. Es estudio se realizará desde el punto de vista cualitativo y cuantitavivo de sales solubles.
En el primer caso abarcaremos las sales que provienen de ácidos fuertes y bases fuertes:
Un ejemplo de este tipo de sal es el cloruro de sodio, NaCl, y se forma por la siguiente reacción:

El cloruro de sodio es conocido también como sal común, y es muy empleado en la cocina de nuestros hogares para dar sabor a los alimentos y en algunos casos para la conservacion de carnes, tambien es utilizado a nivel medicinal para hidratar a las personas y proporcionarles electrolitos, y en diferentes industrias se emplea para la elbaoracion de productos tales como cloro, detergentes, blanqueadores entre otros.

Fuente: @yusvelasquez
La reacción de disociación de esta sal en agua viene dada por:
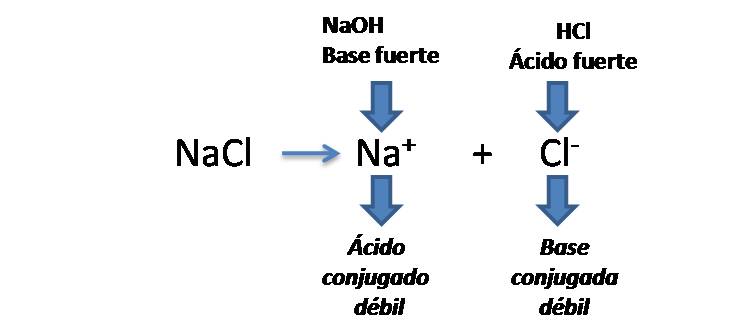
Si analizamos esta reacción, podemos observar que ambos iones Na+ y Cl- proceden de especies fuertes, por lo que son ácidos y bases débiles y por ello no tienen tendencia a reaccionar con el agua , por tanto no tienen efecto significativo en el pH de la solución.
Cálculo del pH
En este caso el pH de la solución depende del aporte de H3O+ proveniente del agua y se espera que sea neutro, es decir, igual a 7. Así se tiene que,
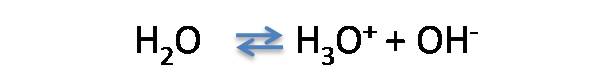
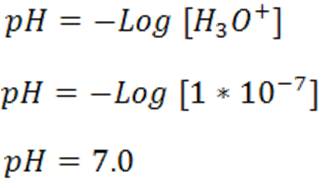
Algunos ejemplos también pueden ser el NaBr, NaI, KNO3 entre otros.
En el segundo caso se tienen las sales provenientes de ácido fuertes y bases débiles:
En esta categoría podemos citar el cloruro de amonio, NH4Cl.
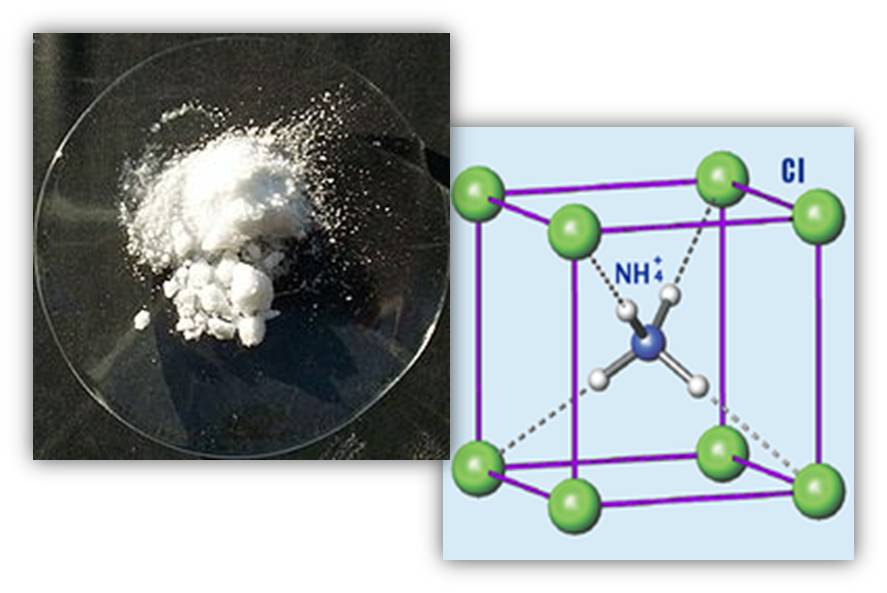
Fuente: Wikipedia.com
Como vemos en la figura, el cloruro de amonio, es una sal de color blanco y altamente soluble en agua, se emplea ampliamente en la produccion de fertilizantes, en la produccion de pilas secas, tratamiento de agua y como aditivo de alimentos.
Ahora para analizar su influencia en el pH de la solucion, debemos comenzar por examinar el anión y el catión de la sal, y determinar si el anión corresponde a la base conjugada de un ácido débil o el catión es el ácido conjugado de una base débil.
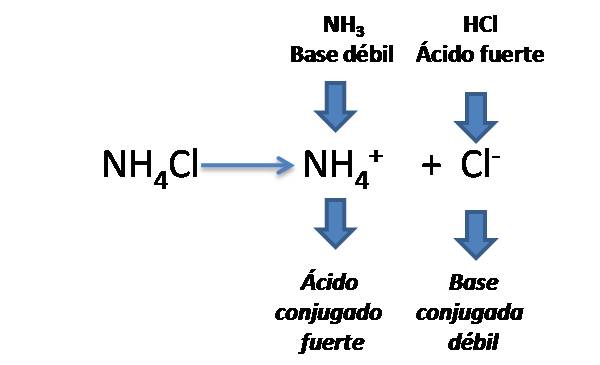
En este caso, el análisis arroja que el catión NH4+ procede de una base débil por tanto tiene fuerte tendencia a hidrolizarse y de ello depende el pH de la solución ya que el ion Cl- proviene de un ácido fuerte tal como se describió en el caso anterior y no se hidroliza.
La reacción de hidrólisis entonces viene dada por

Cálculo del pH
Para calcular el pH de sales independientemente del tipo que sean a excepción de las neutras podemos hacer uso del cuadro de equilibrio, como se muestra en el ejemplo que desarrollaremos a continuación.
Supongamos que se desea calcular el pH de una solución de cloruro de amonio 0.20 mol/L.
Podemos comenzar escribiendo la reacción de hidólisis y completar el cuadro de equilibrio
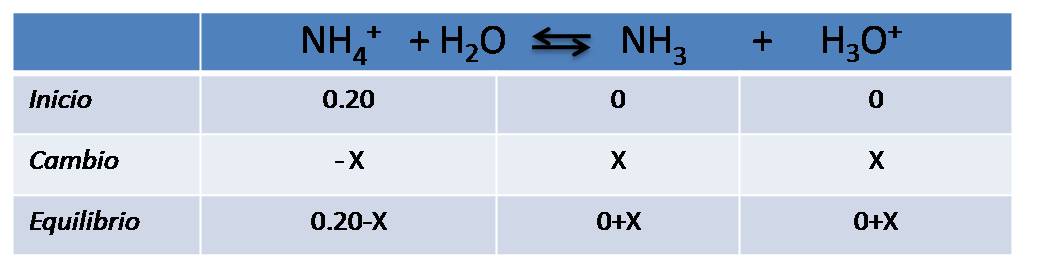
Expresamos la constante de equilibrio (Ka) y calculamos el valor de la constante del ácido conjugado partiendo del valor de la base de donde se formó este ácido. En este caso emplearemos 1.8*10-5 que corresponde a la constante del amoníaco según la bibliografía.
Sustituimos los valores
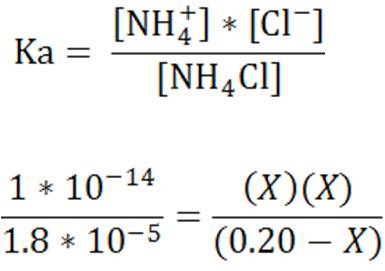
Resolvemos la ecuación
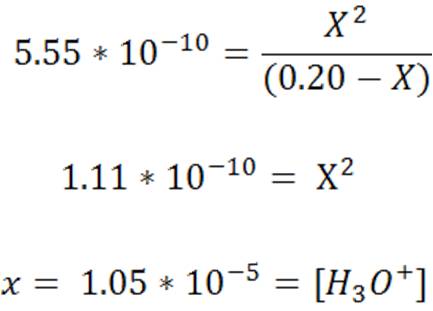
Calculamos el pH con la concentración de H3O+
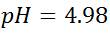
Como vemos el pH resultante es de 4.98 es < 7.0
Podemos concluir entonces, que los cationes ácidos que provengan de bases débiles producen soluciones ácidas.
Entre otros ejemplos se encuentran NH4NO3, NH4Br, NH4NO3 entre otros.
Bueno amigos por los momentos me despido, espero que la información presentada les sea muy útil, en el próximo post estaré describiendo los 2 casos restantes.
¡Gracias por leer, hasta una próxima oportunidad!
Referencias
- Whitten K. y Gailey, K. (1985). Química General. México: Nueva Editoral Interamericana
- Atkins, P. y Jones, L. (2006). Principios de Química. Los caminos del descubrimiento. Buenos Aires: Médica Panamericana.
- Cloruro de sodio. Disponible en chemicalsafetyfacts.org
- Cloruro de amonio. wikipedia.com
Electronic-terrorism, voice to skull and neuro monitoring on Hive and Steem. You can ignore this, but your going to wish you didnt soon. This is happening whether you believe it or not. https://ecency.com/fyrstikken/@fairandbalanced/i-am-the-only-motherfucker-on-the-internet-pointing-to-a-direct-source-for-voice-to-skull-electronic-terrorism
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider supporting our funding proposal, approving our witness (@stem.witness) or delegating to the @stemsocial account (for some ROI).
Please consider using the STEMsocial app app and including @stemsocial as a beneficiary to get a stronger support.
Congratulations @yusvelasquez! You have completed the following achievement on the Hive blockchain and have been rewarded with new badge(s) :
Your next target is to reach 15000 upvotes.
You can view your badges on your board and compare yourself to others in the Ranking
If you no longer want to receive notifications, reply to this comment with the word
STOP