Determinación de la acidez total titulable y el pH en alimentos
En los alimentos podemos encontrar presentes cierta cantidad de ácidos orgánicos que determinan su acidez y pueden influir en diversas características como el sabor y el color, pero además puede determinar la capacidad de los mismos para desarrollar microorganismos perjudiciales, como bacterias y hongos; algo que se conoce desde hace mucho tiempo, por ejemplo el encurtido es una técnica que se utiliza desde antaño para conservar los alimentos. Es por ello que en el análisis químico de alimentos se usan dos conceptos interrelacionados que tratan la acidez: el pH y la acidez valorable. Cada una de estas cantidades se determina analíticamente de forma separada y cada una tiene su propio impacto particular en la calidad de los alimentos.
Tanto en grasas y aceites, jugos y concentrados de frutas y vegetales es fundamental determinar el grado de acidez, ya que el grado de deterioro de los mismos va ligado al valor de esta, por ejemplo, en la leche mientras mayor es el contenido de ácido láctico está más cercana a estar descompuesta, y en las frutas la acidez titulable es un indicativo de su madurez, por lo general mientras más madura esta la fruta menor es el contenido de ácidos. O por otro lado, en productos fermentados como los vinos, la acidez constituye uno de los mejores indicadores de su calidad, siendo un parámetro muy importante en su degustación.
Igualmente el pH nos confiere una referencia del grado de acidez, definido como el –log[H3O]+; su determinación también es importante en la industria de los alimentos, y su valor es utilizado para el control del desarrollo de microorganismos y enzimas en los productos.
 Fuente: @yusvelasquez.
Fuente: @yusvelasquez.Por estas y otras razones es determinante el control de la acidez y el pH en la industria alimenticia. Y aunque el método potenciométrico del pH ha sustituido a muchos otros por su factibilidad y eficiencia, el método para la determinación de la acidez valorable por titulación aún es de los más usados en los laboratorios de análisis químico. Por eso en esta oportunidad quiero compartir con ustedes el método para la determinación de la acidez total titulable.
Acidez en los alimentos
Como ya mencionamos, la acidez en los alimentos se debe a la presencia de ciertos ácidos; por ejemplo, en las frutas la acidez viene dada por ácidos como el cítrico (limón), málico (manzanas) y tartárico (uvas), mientras que los productos cárnicos la acidez viene dada por ácidos como el láctico, en los aceites y grasas se debe a la hidrolisis parcial de los triglicéridos, y el grado de acidez corresponde el porcentaje de ácidos grasos libres, expresados como ácido oleico, y quizás el más común, el ácido acético determina la acidez en el vinagre.
En los alimentos, de forma general se dice que cuando el pH es inferior a 5 es un producto ácido, y en caso contrario que no lo es, sin embargo a nivel industrial se consideran dos tipos de acidez, la natural y desarrollada[1]:
- La acidez natural: debida a la composición natural de los alimentos, por ejemplo la acidez encontrada en las frutas cítricas.

El ácido cítrico le da su acidez natural al limón y otras frutas. Fuente: imagen editada por el autor, fuente original Pxhere.com, CC0
- La acidez desarrollada: esta se debe a la acidificación del alimento mediante un proceso térmico, enzimático o microbiológico. Por ejemplo la acidez de los vinos no solo se debe a la fruta, durante la fermentación y envejecimiento tienen lugar ciertas reacciones que dan lugar a la formación de otros compuestos ácidos.
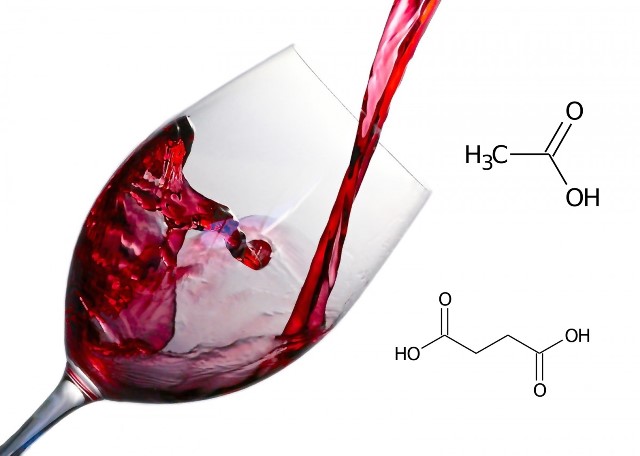
Durante la fermentación del vino se desarrollan ácidos como el acético y succinico. Fuente: imagen editada por el autor, fuente original Pxhere.com, CC0.
La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA por sus siglas en inglés) clasifica los alimentos como acidificados y de baja acidez, y su registro está sometido a un estricto control, ya que cuando se enlata o embotella un producto que requiere refrigeración después de abierto, solo un pH de 4,6 o menos garantiza la ausencia de bacterias dañinas o sus toxinas, sobre todo del mortal Clostridium botulinum[2]; por lo que muchos fabricantes tienen problemas para exportar sus productos a los Estados Unidos si no han hecho una adecuada determinación del pH del producto.
Determinación de la acidez por volumetría
El método procede mediante una valoración ácido-base, la cual tiene muchas aplicaciones prácticas en este tipo de industria, muy especialmente cuando se analizan muestras de origen vegetal porque en la mayoría de estas muestras la acidez viene dada por la presencia de ácidos débiles.
Así, la cantidad de ácidos presentes puede determinarse fácilmente mediante una valoración con una disolución de base fuerte previamente estandarizada, por lo general de hidróxido de sodio, calculándose la concentración en ácido a partir de la reacción de neutralización balanceada, por ejemplo para determinar la acidez acética en el vinagre se procede según la ecuación:
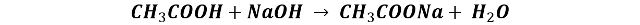
En la que se cumple una reacción mol a mol, por lo que en el punto de equivalencia se cumple que,
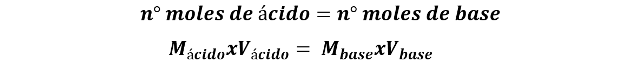
Por lo que, conocida la cantidad de muestra a valorar, la concentración de la base a utilizar y la cantidad de base necesaria para la neutralización, se puede proceder a determinar la concentración del ácido en la muestra.
Método de análisis
Preparación de la muestra
La determinación de la acidez valorable y el pH en muestras de productos alimenticios líquidos como jugos y bebidas claras no representa mayor inconveniente, para productos sólidos, horneados y pastas se debe consultar el método específico.
Acidez total por volumetría
El procedimiento usual para determinar la concentración total de ácidos es tomar una alícuota y titularla con una solución estándar de una base hasta el punto de equivalencia; este punto se detecta haciendo uso de un indicador químico adecuado.
Reactivos:
Hidróxido de sodio 0,1 M
Fenolftaleina 5%
Agua destilada
Procedimiento:
- Se toma una alícuota de 25 mL de la muestra problema y se diluye con agua destilada en un balón aforado de 500 mL.
- Se mezcla bien y con una pipeta se trasvasa una alícuota de 25 mL a una fiola de 250 mL.
- Se agregar tres gotas de fenolftaleína.
- Se enrasa una bureta con la solución de hidróxido de sodio estandarizado.

Muestra en la fiola y valorante en la bureta. Fuente: @yusvelasquez.
- Se procede con la titulación con el hidróxido de sodio, hasta la aparición del primer color rosa permanente.

Titulación de la muestra hasta el cambio de color del indicador. Fuente: @yusvelasquez.
- Y se registra el volumen gastado de hidróxido gastado en la valoración[3].

Punto final de la titulación de una muestra de vinagre usando fenolftaleina como indicador. Fuente: @yusvelasquez.
Determinación del pH, método potenciométrico
- Procedimiento
- Se calibra el pHmetro según las instrucciones del aparato.
- Se deben mantener los electrodos sumergidos en agua destilada y enjuagarse muy bien antes y después de realizar la medición.
- Hacer una medición, agitar la muestra después de tomar la lectura y realizar otra medida; repetir este paso hasta obtener dos lecturas que coincidan.

pHmetro y medición del pH en la muestra. Fuente: @yusvelasquez.
Resultados
Conocido el volumen gastado de Hidróxido de sodio y su concentración, se puede determinar la concentración total de ácidos presentes en la muestra con la ecuación del punto de equivalencia ajustada a la estequiometria:
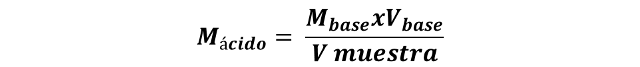
Dónde: M es la concentración molar del ácido o la base respectivamente, Vbase es el volumen gastado de hidróxido de sodio y Vmuestra es el volumen de la muestra valorada.
Al conocer el ácido a valorar se puede emplear su masa molar en el cálculo para expresar la acidez como g/L de determinado ácido.
Interferencias
No existen mayores interferencias con el método, excepto cuando son jugos o muestras que presentan color, en estos casos se procura incrementar la cantidad de indicador para hacer visible el cambio de color en la muestra. En muestras que contienen dióxido de carbono, como vinos y bebidas gaseosas, conviene desgasificar la muestra para evitar errores al añadir la acidez del gas carbónico.
Conclusión y aporte
La acidez y el pH son parámetros de especial control en la industria del procesamiento de alimentos, no solo porque puede afectar el color y el sabor de los alimentos, sino también porque es una medida de la estabilidad y grado de conservación de los mismos. Además, muchos entes regulan con estricto control la seguridad de los alimentos, por lo que asegurar la ausencia de microorganismos mediante el ajuste del pH del producto es esencial.
El presente artículo permite dar a conocer el método analítico para la determinación de la acidez en muestras líquidas de alimentos, como jugos, vinos y encurtidos mediante la volumetría de neutralización usando fenolftaleína como indicador y el pH mediante medidas potenciométricas, técnicas muy utilizadas en los laboratorios de análisis químico de alimentos, sirviendo como una guía para los estudiantes de química analítica que requieren información del mismo y como un medio para socializar la importancia de la determinación de la acidez en los alimentos.
Bueno amigos, hasta aquí el presente post, espero que la información presentada les sea de mucha utilidad, recordándoles que un resultado confiable en el análisis químico depende de aplicar la técnica analítica apropiada. ¡Hasta un próximo post!
Referencias
- Wikipedia.com. Acidez
- Statman, R. (2012). Regulaciones Estadounidenses para la Exportación de Alimentos de Baja Acidez o Acidificados
- Ramírez D., Velásquez, Y., Lugo, O., Ferreira, M., Quintero, M. (2015). Guías prácticas del laboratorio de Química Analítica Universidad Nacional Experimental Francisco de Miranda.
Hola estimada @yusvelasquez, un gusto saludarla de nuevo, en el artículo anterior le comentaba que el pH es determinante en muchos procesos, y usted en la presente entrega describe de una manera clara la importancia del pH en ciertos procesos, además de ello socializa los métodos para su determinación, lo cual me parece de mucho valor, ya que nos educa al respecto y aclara algunas dudas. Espero se encuentre bien y seguimos leyendonos !👍
Saludos estimado @amestyj, el gusto es mio de que vuelva a pasar por mi blog, me alegra que se vea el proposito del post, contribuir en la educación, ya que es un método muy útil y aplicable en diversos tipos de muestras y aclara la influencia de la acidez en muchas de las propiedades de los alimentos. Nos sguimos leyendo!
Esta influencia de la acidez en los alimentos nos permite medir un intervalo de consumo de estos. Es interesante ver como el pH influye en otros organismos y como los transforma de diferentes maneras. ¡Saludos!
Curador: @universoperdido
Saludos amigos de @alebrijes, gracias por el apoyo. El pH y la acidez son determinante en muchas características y propiedades de los alimentos, especialmente en ello, controlan la presencia de microorganismos e influyen en el intervalo de consumo.
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider supporting our funding proposal, approving our witness (@stem.witness) or delegating to the @stemsocial account (for some ROI).
Thanks for using the STEMsocial app and including @stemsocial as a beneficiary, which give you stronger support.
Muchas gracias amigos!
Muy importante para considerarse sobre todo en la preservación de los alimentos como por ejemplos los lácteos, que solo toleran un grado mínimo de acidez para poder procesarse en otros subproductos, un post muy valioso gracias por compartir. Saludos
Así es, en los productos lácteos es muy importante el control de la acidez y el pH, se que en la leche se debe controlar desde su recolección hasta la entrega, ya que si el pH disminuye es indicativo de la degradación del producto ocasionado por baterias que producen ácido láctico. Gracias a ti por pasar a leer @carlos84, saludos!
Toda una clase sobre acidez titulable e iónica. Muy útil como guía. Saludos @yusvelasquez.
Saludos @capp. Muchas gracias, esa es la intención, proveer una guía útil sobre el tema. Gracias por pasar a leer