¿Se puede hervir agua en un plato de cartón?
Por insólita que parezca la pregunta la respuesta es sí, sí se puede hacer hervir agua en un recipiente hecho de papel o cartón. Y si no me creen se los demuestro en el siguiente video.
En este experimento se pone a prueba una propiedad conocida como calor específico. Y a pesar de lo que pueda parecer, no hace referencia a la temperatura de ebullición o combustión de algo, es un concepto más amplio que tiene que se relaciona con la capacidad que tienen las sustancias para almacenar energía calorífica. Como habrán notado en el video, no todas las sustancias se calientan a la misma velocidad, el recipiente de cartón, el agua e incluso el vapor tiene un calor específico diferente, por eso se calientan de diferente forma.

La estufa, el plato y el agua tienen diferentes calores específicos. Fuente: @emiliomoron.
Pero, ¿qué es el calor específico?
El calor específico es una magnitud relacionada con la capacidad calorífica las sustancias, esta última es la cantidad de calor que puede almacenar una sustancia antes de cambiar de temperatura. Matemáticamente hablando se dice que es la cantidad de calor, Q, necesario para producir en un sistema un aumento de temperatura en una unidad[1].
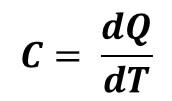
De modo que, la cantidad de calor, Q, que se necesita para producir en un sistema un cambio de temperatura, ∆T, se puede expresar como:
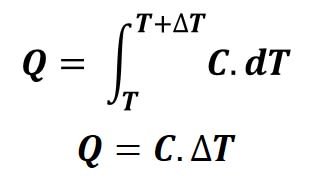
La capacidad calorífica es una propiedad extensiva, lo que quiere decir que es proporcional a la cantidad de materia del sistema, por lo que suele ser más conveniente expresar la correspondiente magnitud por unidad de masa, es decir, la cantidad de calor que hay que suministrar a una cantidad de masa, m, de una sustancia para elevar su temperatura en una unidad, es decir, el calor que se necesita para que una determinada cantidad de masa eleve su temperatura un grado más, siendo esta magnitud el calor específico, c.
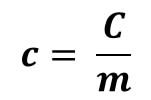
La cantidad de energía que se absorbe se expresa en joules (J) o también puede expresarse en calorías (cal), siendo las unidades del calor especifico más comunes J/g.K. o cal/g.°C.
Volviendo a nuestro experimento, ¿Cómo influye el calor específico para que el plato no se queme?
Algunas sustancias se calientan rápidamente, quizás hayamos notado que un trozo de metal que se acerca a una fuente de calor se calienta casi al tacto mientras que un trozo de madera o goma demora mucho más en calentarse. El agua es una de las sustancias que se calienta lentamente, tiene una alta capacidad de calor específico por lo que requiere más energía para elevar la temperatura. El agua siempre nos sorprende con sus propiedades anómalas.
Por ejemplo, el agua posee una capacidad calorífica de 4181 J/Kg.°C, considerablemente alta respecto a otras sustancias. En el caso del video, podemos apreciar que para calentar el agua esta debe absorber el calor de llama de la cocina, y hervirá cuando alcance su punto de ebullición (100 °C), en el proceso, retira gran cantidad de calor del cartón, por lo que este no puede empezar a quemarse. Y aun cuando el agua alcanza su punto de ebullición, cualquier cantidad de calor suministrada es utilizada para producir el cambio de fase, es decir, para vaporizar el agua, por lo que mantendrá una temperatura constante de 100 °C y el papel tiene una temperatura de ignición de 232 °C[2], mucho mayor que la temperatura de ebullición del agua, así que no se alcanzará esta temperatura hasta que toda el agua colocada en el recipiente se haya evaporado.

Gracias al calor específico del agua el cartón no se quema. Fuente: @emiliomoron.
El agua es tan común y a la vez tan importante que tiene una forma especial de identificar la cantidad de energía necesaria para elevar la temperatura de un gramo de agua en un °C, esto equivale a una caloría.
¿Qué significado tiene que el calor específico sea tan alto?
Un alto calor especifico quiere decir que una sustancia tendrá mayor resistencia para aumentar su temperatura, por lo que puede absorber mayor energía, es decir, tendríamos que calentar por mucho más tiempo el agua que una sustancia con menor calor específico para notar un cambio en su temperatura. Así, por ejemplo, los metales como el aluminio y el hierro tienen un calor específico tan bajo que en al exponerlos al fuego se calentaran casi al instante, pero incluso, el hierro se pondrá al rojo vivo antes que el aluminio. En la siguiente tabla podemos comparar el calor específico de algunas sustancias.
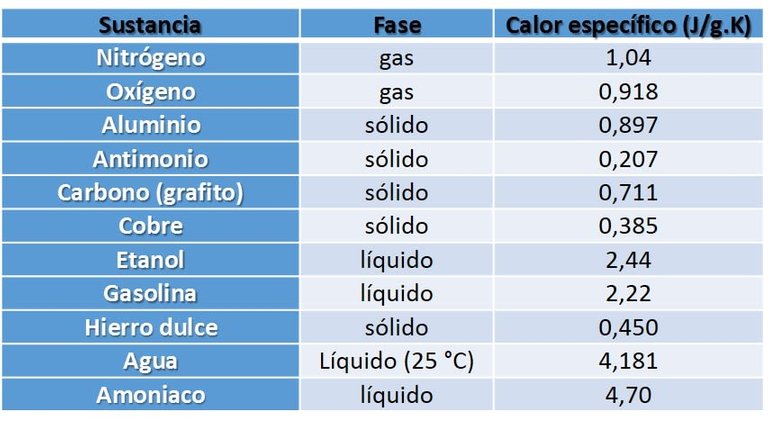 Fuente: datos tomados de wikipedia.com[3].
Fuente: datos tomados de wikipedia.com[3].El alto calor específico del agua explica porque las masas de agua cambian su temperatura de forma más lenta que las rocas y el suelo en la superficie terrestre, actuando como reguladores del flujo de calor entre la litosfera y la atmosfera, lo cual es fundamental para la regulación del clima en nuestro planeta[4].
Tan solo pensemos que cuando vamos a la playa en un día soleado, aunque en el ambiente se perciba mucho calor, el agua siempre tiene una temperatura más fresca. Lo notamos al caminar por la arena caliente y luego sentir el agua fría en nuestros pies; eso se debe a que la arena tiene una menor capacidad de calor específico, y como el sol emite una cantidad de energía más o menos constante, la arena se calienta mucho más rápido que el agua.
 La arena y el agua tienen diferentes calores específicos. Fuente: Pixinio.com, imagen de dominio público
La arena y el agua tienen diferentes calores específicos. Fuente: Pixinio.com, imagen de dominio públicoEste aspecto también es importante para la vida acuática, gracias a ello por ejemplo, el océano puede percibir gran cantidad de radiación solar, y el agua apenas se calentara en un grado apreciable durante todo el día, con lo que se mantiene una diferencia térmica que no afectará el ecosistema marino.
Por otro lado, una vez que el agua ha aumentado su temperatura deberá liberar una gran cantidad de energía para enfriarse, para ello ahora el flujo de calor será contrario, calentando en el proceso las masas de aire en la ambiente circundante, manteniendo así un poco más cálidas las noches en las zonas costeras.
¿y a que se debe este alto calor especifico del agua?
Si nos hemos fijado en la tabla anterior, el amoniaco, además del agua, posee un alto calor específico. Estos valores tan únicos se debe a que estas sustancias pueden formar puentes de hidrogeno. Estas fuerzas intermoleculares son la explicación de muchas de las propiedades anómalas que observamos en el agua, como la disminución de la densidad al solidificarse. Como sabemos, las moléculas deben absorber energía para romper los enlaces y producir un cambio de fase, en el caso del agua las moléculas están fuertemente unidas entre sí, la energía máxima en un puente de hidrogeno entre dos moléculas de agua es de aproximadamente 23 kJ/mol, sin considerar las interacciones electrostáticas con otras moléculas; por lo tanto, es necesario suministrar mucha energía para hacer que las moléculas de agua se separen, y mientras permanezcan juntas, no podrán vibrar y para aumentar su temperatura las moléculas de agua deben aumentar su vibración, mientras tanto, seguirán acumulando energía.
En este sentido, toda la energía que se suministra para calentar el agua se divide entre la ruptura de los enlaces, que se forman y rompen constantemente, lo que los hace difíciles de romper. La razón de esta dificultad está en la estructura de la molécula de agua, como está formada por dos átomos de hidrogeno y un átomo de oxígeno que tiene dos pares de electrones libres, es capaz de formar cuatro enlaces entre moléculas. El número total de enlaces fluctúa con el tiempo y depende de la temperatura, pero a partir de simulaciones se ha estimado que en promedio se cada molécula de agua participa en 3,5 enlaces por puentes de hidrógeno[5].
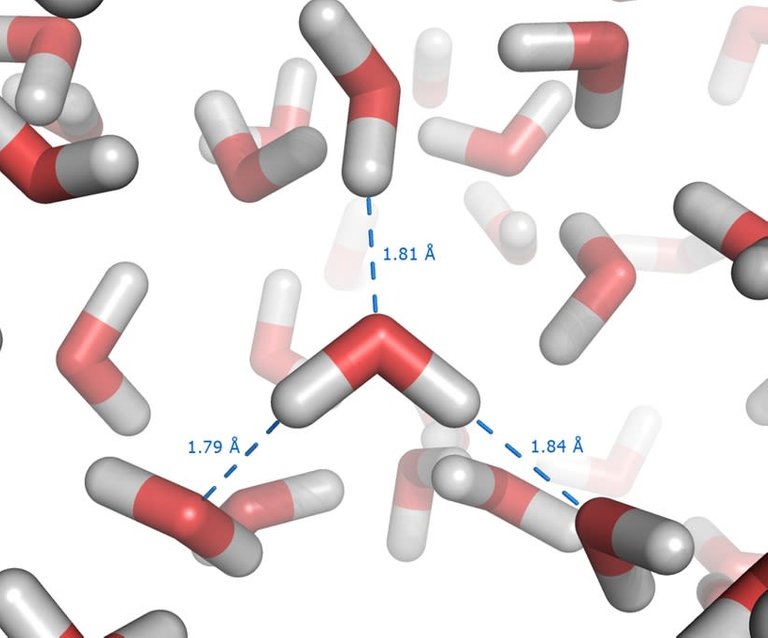
Simulación de la formación de enlaces por puente de hidrógeno entre moléculas de agua. Fuente: Wikipedia.com, imagen CC BY-SA 3.0.
Como ven, este experimento deja en evidencia esta extraordinaria propiedad, que le permite a las grandes masas de agua ser un medio de transporte de energía y contribuir con la regulación de la temperatura en nuestro planeta. Además de ser una fácil experiencia para realizar con estudiantes de secundaria y demostrar la capacidad calorífica de las sustancias.
Bueno amigos, espero que les haya gustado mi post, gracias por pasar a leer, hasta el próximo!
Referencias
- Wikipedia.com. Capacidad calorífica.
- Wikipedia.com. Temperatura de ignición.
- Wikipedia.com. Calor específico.
- Rodríguez, J.M. y Marín, R. (1999). Fisicoquímicas de aguas. Ed. Díaz de Santos, España.
- Wikipedia.com. Fuerza por puente de hidrógeno.

Las formulas, reacciones y estructuras químicas indicadas fueron elaboradas por el autor en Microsoft PowerPoint.
Y amigo lector, si desean consultar más artículos de interés científico y de excelente calidad, visiten la etiqueta #STEM-espanol, este es un proyecto adscrito a la comunidad académica y científica #STEMSocial en Hive, una comunidad que promueve contenido científico en las áreas de Ciencia, Tecnología, Ingeniería y Matemáticas.
¡Felicidades! Esta publicación obtuvo upvote y fue compartido por @la-colmena, un proyecto de Curación Manual para la comunidad hispana de Hive que cuenta con el respaldo de @curie.
Si te gusta el trabajo que hacemos, te invitamos a darle tu voto a este comentario y a votar como testigo por Curie.
Si quieres saber más sobre nuestro proyecto, acompáñanos en Discord: La Colmena.
Gracias amigos de @la-colmena
This post was shared in the #spanish-curation channel in the Curation Collective Discord community for curators, and upvoted and reblogged by the @c2-spanish community account after manual review.
@c-squared runs a community witness. Please consider using one of your witness votes on us here
Muchas gracias equipo de @c-squared
Muchas gracias por el apoyo @mayvileros!
De nada cariño. Feliz noche.
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider supporting our funding proposal, approving our witness (@stem.witness) or delegating to the @stemsocial account (for some ROI).
Thanks for using the STEMsocial app, which gives you stronger support. Including @stemsocial as a beneficiary could yield even more support next time.
Vaya es una propiedad muy interesante de los materiales, el calor específico o la resistencia a aumentar su temperatura. Creo que tiene cierta analogía a la rigidez en elementos estructurales, la cual es una propiedad que mide la resistencia a la deformación de los mismos.
Puede que con este post le salves la vida a alguien en una situación de supervivencia donde solo dispone de un plato de cartón para hervir el agua jeje, se puede sobrevivir gracias a la ciencia. Gracias por compartir, saludos! @emiliomoron
Saludos @acont. Ciertamente interesante esta propiedad, y como esta el agua tiene muchas características que sorprenden. Es muy posible la analogía, habría que revisarlo.
Y bueno, la verdad podría ser un recurso de supervivencia jajaja, si sólo se tiene un vaso o plato de cartón y se necesita por ejemplo, desinfectar algo de agua.