Experimentárium - časť 3. - Lávová lampa
V dnešnej časti Experimentária ešte posledný krát využijeme reakciu octu a sódy bikarbony, k chemickým reakciám už ale tentokrát pridáme aj trochu fyziky. Konkrétne využijeme povrchové napätie, viskozitu a rozdielne hustoty rôznych látok k tomu, aby sme z nášho bublinkujúceho mixu vytvorili efektnú lávovú lampu.

Všetci zrejme viete, že keď nalejeme ľubovoľný kuchynský olej do nádoby s vodou, olej sa s vodou nezmieša, ale ostane "plávať" na jej hladine.
Vysvetlenie toho, prečo by mal olej ostať plávať na hladine vody, je jednoduché. Olej má jednoducho menšiu hustotu ako voda (ľudovo povedané, je "ľahší"). Na jej povrchu preto ostane plávať podobne, ako napr. kus dreva.
Prečo sa ale s vodou nezmieša, resp. sa v nej nerozpustí? Odpoveď na túto otázku súvisí s povrchovým napätím vody (a samozrejme aj oleja, kde je ale tento efekt výrazne slabší). Na každú molekulu vody, ktorá sa nachádza v jej objeme, totiž príťažlivou silou pôsobia ostatné molekuly vody nachádzajúce sa okolo nej. Pokiaľ je táto molekula v objeme vody, tieto sily sú zo všetkých strán rovnaké, takže sa navzájom vykompenzujú a výsledné silové pôsobenie je nulové. Ak sa ale táto molekula nachádza na povrchu vody (t.j. na rozhraní voda/vzduch), príťažlivou silou na ňu pôsobia iba molekuly vody na jednej strane povrchu, ako možno vidieť na obrázku nižšie. To spôsobí, že povrchové molekuly sú priťahované smerom do vnútra, teda do objemu vody.
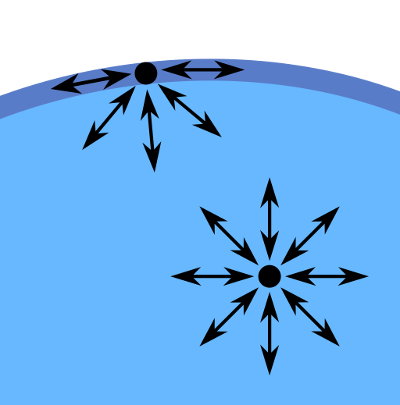
Dôsledkom tohto celého je, že voda sa snaží minimalizovať svoj povrch [1]. Vďaka tomu má napr. kvapka vody snahu zaujať tvar gule, ktorá má pri danom objeme minimálnu plochu povrchu.
Na rozhraní vody a oleja na molekuly vody pôsobia príťažlivou silou aj molekuly oleja na druhej strane rozhrania, ale ich silové pôsobenie je v porovnaní s molekulami vody výrazne slabšie. Výsledok je preto podobný ako v prípade rozhrania vody so vzduchom - voda sa snaží minimalizovať plochu rozhrania. Dôsledkom je, že celý objem vody a oleja sa od seba oddelí, pretože takto má ich rozhranie najmenšiu plochu. Rozdelenie oleja na kvapôčky, prípadne jeho rozpustenie vo vode na jednotlivé molekuly by malo za následok obrovské zväčšenie plochy rozhrania voda-olej.
No a teraz začnime už aj trochu experientovať
To, že olej sa s vodou nezmieša a ostane plávať na hladine, sme si už vysvetlili. Čo sa ale stane, keď do nádoby najprv nalejeme olej a až následne na neho nalejeme vodu? Voda, keďže má väčšiu hustotu, sa bude snažiť dostať na dno oleja. Vyššie spomínané povrchové napätie a vysoká viskozita oleja jej tento proces ale trochu skomplikujú, takže tam nepadne naraz "ako kameň", ale bude na dno prechádzať postupne, pričom sa môžu dočasne vytvoriť aj "kvapky" vody v oleji a naopak. To si môžte za pár sekúnd vyskúšať aj sami, ale ak nechcete zbytočne plýtvať olejom, dá sa to vidieť napr. aj na videu nižšie:
Týmto sme sa už dostali celkom blízko k našej vytúženej lávovej lampe. Musíme ale ešte nejakým spôsobom zabezpečiť, aby sa tieto "kvapky" vody následne dostali späť na povrch a celý proces sa opakoval. A práve to dosiahneme pomocou starej známej rekacie octu a sódy bikarbony. Stačí totiž zopakovať to isté, akurát s tým rozdielom, že namiesto vody použijeme ocot a na dno nádoby nasypeme trochu sódy bikarbony... a lávová lampa je na svete.
Postup experimentu je nasledovný:
Ak chceme mať naozaj "lampu", sklenenú nádobu, ktorú budeme ďalej používať, postavíme na zdroj svetla. Tým získame efektné podsvietenie. Postačí napr. aj svetlo z mobilného telefónu.
Do nádoby nasypeme sódu bikarbonu. Jej množstvo nie je veľmi dôležité, takže sa riadime heslom "primerane".
Následne nádobu naplníme takmer do plna kuchynským olejom (nemusí byť zrovna extra virgin ;)
Pomaly začneme prilievať ocot. Znova primerane, radšej menej ako viac. Pre efektnejšie "divadlo" môžme ocot ešte predtým zafarbiť potravinárskym farbivom (dá sa kúpiť vo väčšine potravín).
Hotovo, lávová lampa je na svete.
V ideálnom prípade by to nakoniec malo vyzerať nejak takto:
Pozrime sa ale ešte bližšie na to, čo sa to tam vlastne deje. Po naliatí octu do oleja začne ocot klesať ku dnu. V momente ako klesne na dno ale začne reagovať so sódou bikarbonou, ktorá sa nachádza na dne nádoby. To vytvorí pomerne veľké množstvo bubliniek CO2, ako sme si ukázali v prvej časti Experimentária. Kvôli povrchovému napätiu vody (octu) aj oleja je energeticky najvýhodnejšie, keď sa tieto bublinky, ktoré sa chcú dostať na hladinu, sústredia na ich rozhraní. Pri svojej púti na hladinu oleja preto so sebou vynesú aj kvapku octu, ktorá sa obalená bublinkami stane "ľahšou" ako olej. V momente ako sa táto kvapka dostane na hladinu, sa ale niektoré z bubliniek uvoľnia do ovzdušia. Kvapka octu, aj keď na nej ešte niekoľko bubliniek ostane "prichytených" sa tým opät stane "ťažšia" ako olej a začne znova klesať ku dnu. Následne sa celý proces, ktorý je pomerne pomalý vďaka vysokej viskozite oleja, zopakuje. Kvapky octu teda budú putovať olejom hore na hladinu a potom späť na dno, až kým sa nevyčerpá všetka kyselina octová alebo sóda bikarbona.
Zdroj úvodého obrázku: www.youtube.com (posledné video v článku)
Literatúra:
[1] https://sk.wikipedia.org/wiki/Povrchové_napätie
Predchádzajúce časti Experimentária:
Experimentárium - časť 2. - Horúci ľad
Experimentárium - časť 1. - Ocot a sóda bikarbona
Nestíhám, takže si tu zatím jen odložím Tipáka a na pokus mrknu později ;)
@tipu curate
Upvoted 👌 (Mana: 24/44) Liquid rewards.
Ďakujem :)
Yay! 🤗
Your content has been boosted with Ecency Points, by @timehacker.
Use Ecency daily to boost your growth on platform!
Support Ecency
Vote for new Proposal
Delegate HP and earn more
!1UP
Thank you :)
You have received a 1UP from @fsc69!
@stem-curator, @vyb-curator, @pob-curatorAnd they will bring !PIZZA 🍕
Learn more about our delegation service to earn daily rewards. Join the family on Discord.